提出元素周期律并绘制了第一张元素周期表的化学家是( )
A.戴维 B.侯德榜 C.道尔顿 D.门捷列夫
下列有关实验室制取蒸馏水的实验装置与操作的说法中,错误的是( )
A.冷凝管中水流方向是从下口进入,上口排出
B.温度计的水银球应插入蒸馏烧瓶的自来水中
C.实验中需要在烧瓶中加入几粒碎瓷片,防止出现暴沸现象
D.蒸馏烧瓶必须垫加石棉网加热
下列分离方法错误的是( )
A.除去混在植物油中的水——倾倒 B.除去粗盐中的泥沙——过滤
C.用乙醚提取中草药中的有效成分——萃取 D.除去氯气中的氯化氢气体——洗气
下列实验操作正确的是( )
| 编号 | 实验 | 操作 |
| A | 制备氢氧化铝凝胶 | 向氯化铝溶液中加入过量的氢氧化钠溶液 |
| B | 配制一定浓度的氯化钾溶液100mL | 将称好的氯化钾固体放入100 mL容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 灼烧铝片 | 将金属铝表面用砂纸仔细打磨,除去氧化膜后,在酒精灯火焰上灼烧,有液态铝滴落 |
| D | 制备Fe(OH)3胶体 | 向盛有沸水的烧杯中滴加饱和FeCl3溶液,继续加热至溶液呈现红褐色 |
A.A B.B C.C D.D
下列化学用语正确的是( )
A.H2S的电子式:![]() B.S2-结构示意图:
B.S2-结构示意图: 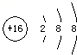
C.Na2O2的电子式:![]() D.CCl4的电子式:
D.CCl4的电子式:![]()
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
A.标准状况下,18gH2O中含有的分子数目为NA
B.标准状况下,2.24LCl2与足量铁粉反应转移电子数目为0.2NA
C.46gNO2和N2O4混合气体中含有的原子数目为3NA
D.1molN2与4molH2混合充分反应,生成NH3分子的数目为2NA
0.05mol某金属单质与足量的盐酸反应,放出1.12LH2(标准状况),并转变为具有Ne原子的电子层结构的离子,该金属元素在元素周期表中的位置是( )
A.第三周期、ⅠA族 B.第三周期、ⅡA族
C.第四周期、ⅠA族 D.第四周期、ⅡA族
如下图所示每条折线表示周期表IVA〜VII中的某一族元素氢化物,其中a点代表的是
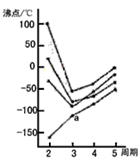
A.H2S B.HCl
C.PH3 D.SiH4
下列说法正确的是
A.离子化合物中一定含有金属元素
B.构成物质的分子中一定含有化学键
C.非极性键也可能存在于离子化合物中
D.共价化合物中可能含有离子键
下列关于能量转化的说法中正确的是( )
A.给手机充电时:化学能转化为电能
B.铅蓄电池的放电过程:电能转化为化学能
C.氢气在氧气中燃烧:化学能转化为热能和光能
D.植物的光合作用:生物质能(化学能)转化为光能(太阳能)
已知反应A+B= C+D的能量变化如下图所示,下列说法正确的是

A.该反应是放热反应
B.只有在加热条件下才能进行
C.反应物的总能量高于生成物的总能量
D.反应中断开化学键吸收的总能量高于形成化学键放出的总能量
有关电化学知识的描述正确的是
A.CaO+H2O=Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能
B.原电池的两极一定是由活动性不同的两种金属组成
C.从理论上讲,任何能自发进行的氧化还原反应都可设计成原电池
D.原电池工作时,正极表面一定有气泡产生
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中,以下叙述正确的是( )
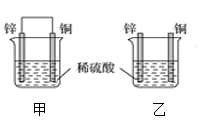
A.两烧杯中溶液的pH均增大
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中铜片表面均无气泡产生
D.产生气泡的速度甲比乙慢
在下列过程中,需要加快反应速率的是( )
A.食物变质 B.合成氨 C.钢铁腐蚀 D.塑料老化
锌与过量的稀盐酸反应,为了加快反应速率,又不影响生成氢气的总量,可以采取的措施是( )
A.加入浓盐酸 B.加入一定量CuSO4固体 C.加入适量的水 D.降低温度
下列表示的是化学反应 A+2B=C+D 在不同条件下的反应速率,其中最快的是
A.v(A)=0.3mol∙L-1∙s-1 B.v(B)=0.5mol∙L-1∙s-1
C.v(C)=0.25mol∙L-1∙s-1 D.v(D)=0.2mol∙L-1∙s-1
在一定条件下,对于密闭容器中进行的可逆反应:H2(g)+I2(g)![]() 2HI(g),达到化学平衡状态的标志是( )
2HI(g),达到化学平衡状态的标志是( )
A.正、逆反应速率都等于零 B.H2、I2的浓度相等
C.HI、H2、I2在容器中共存 D.HI、H2、I2的浓度均不再变化
下列不属于高分子化合物的是( )
A.纤维素 B.聚氯乙烯 C.淀粉 D.油脂
下列变化属于物理变化的是( )
A.石油分馏 B.煤的液化 C.蛋白质变性 D.石油裂化
下列各组有机物中,仅使用溴水不能鉴别出的是
A.乙烯、乙炔 B.苯、四氯化碳
C.乙烷、乙烯 D.苯、酒精
用如下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )

A.上下移动①中铜丝可控制SO2的量
B.②中选用品红溶液验证SO2的生成
C.③中选用NaOH溶液吸收多余的SO2
D.为确认CuSO4生成,向①中加水,观察颜色
下列有关海水综合利用的说法正确的是
A.利用电解的方法可以从海水中获取淡水
B.海水中含有钾元素,只需经过物理变化可以得到钾单质
C.海水蒸发制海盐的过程只发生了化学变化
D.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。X和Z为同主族元素,由X、Z两种元素形成的化合物是形成酸雨的主要物质。下列说法不正确的是( )
A.X的简单氢化物的热稳定性比W的强
B.Y的简单离子与X的具有相同的电子层结构
C.Z与Y属于同一周期
D.W、X、Y、Z原子的核外最外层电子数的总和为20
O3在水中易分解。一定条件下,起始浓度均为0.0216mol/L的O3溶液,在不同的pH、温度下,发生分解反应,测得O3浓度减少一半所需的时间(t)如下表所示:
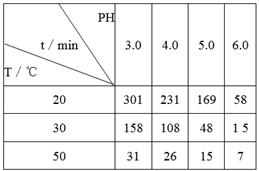
下列判断不正确的是
A.实验表明,升高温度能加快O3的分解速率
B.pH增大能加速O3分解,表明OH-可以对O3的分解起催化作用
C.在30℃、pH=4.0时,O3的分解速率为1.00×10-4mol/(L·min)
D.据表中的规律可推知,O3在下列条件下的分解速率v(40℃、pH=3.0)>v(30℃、pH=7.0)
乙酸乙酯是无色具有水果香味的液体,沸点为77.2℃,实验室某次制取它用冰醋酸14.3mL、95%乙醇23mL,还用到浓硫酸、饱和碳酸钠以及极易与乙醇结合成六水合物的氯化钙溶液,主要装置如图所示:
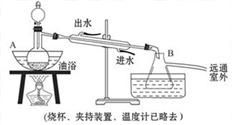
实验步骤:
①先向A中的蒸馏烧瓶中注入少量乙醇和浓硫酸后摇匀,再将剩下的所有乙醇和冰醋酸注入分液漏斗里待用。这时分液漏斗里冰醋酸和乙醇的物质的量之比约为5∶7。
②加热油浴保温约135 ℃~145℃
③将分液漏斗中的液体缓缓滴入蒸馏烧瓶里,调节加入速率使蒸出酯的速率与进料速率大体相等,直到加料完成。
④保持油浴温度一段时间,至不再有液体馏出后,停止加热。
⑤取下B中的锥形瓶,将一定量饱和Na2CO3溶液分批少量多次地加到馏出液里,边加边振荡,至无气泡产生为止。
⑥将⑤的液体混合物分液,弃去水层。
⑦将饱和CaCl2溶液(适量)加入到分液漏斗中,振荡一段时间后静置,放出水层(废液)。
⑧分液漏斗里得到的是初步提纯的乙酸乙酯粗品。
试回答:
(1)实验中浓硫酸的主要作用是_________________________。
(2)用过量乙醇的主要目的是____________________________。
(3)用饱和Na2CO3溶液洗涤粗酯的目的是_______________________。
(4)用饱和CaCl2溶液洗涤粗酯的目的是_______________________。
(5)在步骤⑧所得的粗酯里还含有的杂质是_____________________。
常温下氨气能被氯气氧化生成N2,化工厂常用此法检验管道是否泄漏氯气。某探究小组在实验室对氨气与氯气反应进行了探究,回答下列问题。
Ⅰ.氨气的制备
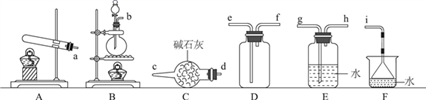
(1)氨气的发生装置可以选择上图中的________(填大写字母),反应的化学方程式为____________________________________。
(2)欲收集一瓶干燥的氨气,选择上图中的装置,按气流方向写出其接口的连接顺序:发生装置管口→________(填小写字母)。
Ⅱ.氯气与氨气的反应
室温下,用收集到的氨气按下图所示装置进行实验(实验前k1、k2关闭)。
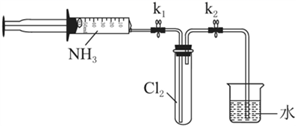
(3)打开k1,缓缓推动注射器活塞,向试管中注入约3倍于氯气体积的氨气,关闭k1,恢复室温。试管中可观察到的现象是________。发生反应的化学方程式为________。
(4)再打开k2,可观察到的现象是________。