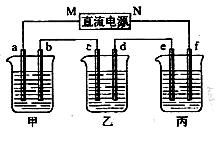
 右图所示装置中, 甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
右图所示装置中, 甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为 极;②电极b上发生的电极反应为 ;
③列式计算电极b上生成的气体在标准状态下的体积: ;
④电极c的质量变化是 g;⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:甲溶液 ;乙溶液 ; 丙溶液 ;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
答案
(1)①正极 ②4OH--4e-=2H2O + O2↑。
③水减少的质量:![]()
生成O2体积:![]()
④16g
⑤碱性增大,因为电解后,水量减少溶液中NaOH浓度增大
酸性增大,因为阳极上OH-生成O2,溶液中H+离子浓度增大
酸碱性大小没有变化,因为K2SO4是强酸强碱盐,浓度增加不影响溶液的酸碱性
(2)能继续进行,因为CuSO4溶液已转变为H2SO4溶液,反应也就变为水的电解反应。