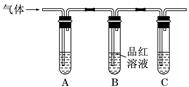
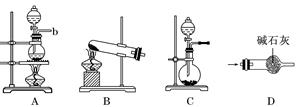
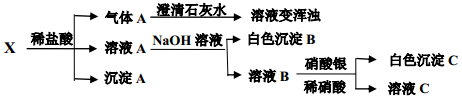
有关混合物分离与提纯的方法广泛应用于实验研究和生产。
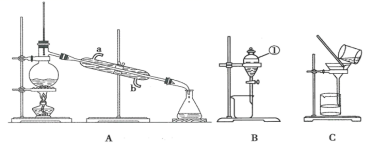
根据图装置回答下列问题:
( 1 )若用装置 A 分离 CCl 4 和溴苯的混合物 ( 已知 CCl 4 和溴苯互溶,沸点分别为 76.75 ℃和 156.2 ℃,在实验时冷却水从冷凝管的 ___ ( 填 “a” 或 “b”) 端通入;在蒸馏操作中,在蒸馏烧瓶中加入沸石 ( 或碎瓷片 ) 的作用是 ___ 。
( 2 )装置 B 中仪器 ①的名称是 ___ ,用装置 B 分离混合物时,为使液体顺利流下,应进行的操作是 ___ 。
( 3 )粗盐中含少量泥沙、 CaCl 2 、 MgCl 2 及硫酸盐,将粗盐溶解后,先用装置 c 将泥沙除去,再检验滤液中的 SO ,检验滤液中 SO
的实验操作和现象是 ___ 。
( 4 )若配制 0.5mol·L -1 硫酸溶液 500mL 则所需质量分数为 98 %、密度为 1.84g·cm -3 的浓硫酸的体积为 ___ mL( 计算结果保留一位小数 )
答案
b 防止暴沸 分液漏斗 先将分液漏斗颈上的玻璃塞打开(或先使塞上的凹槽对准漏斗上的小孔),再将分液漏斗下面的活塞拧开 取少量滤液于小试管中,滴加足量盐酸酸化无明显现象,再加入 BaCl 2 溶液,若有白色沉淀产生,说明含有 SO 13.6
【分析】
A 是蒸馏装置, B 是萃取分液装置, C 是过滤装置,以此解答。
【详解】
( 1 )用装置 A 分离 CCl 4 和溴苯的混合物 , 为蒸馏 , 在实验时冷却水从冷凝管的 b 端通入;在蒸馏操作中,在蒸馏烧瓶中加入沸石 ( 或碎瓷片 ) 的作用是:防止暴沸;故答案为: b ;防止暴沸;
( 2 )装置 B 中仪器 ①的名称是分液漏斗 , 用装置 B 分离混合物时 , 为使液体顺利流下 , 需要的操作方法为:先将分液漏斗颈上的玻璃塞打开 ( 或先使塞上的凹槽对准漏斗上的小孔 ) ,再将分液漏斗下面的活塞拧开,故答案为:分液漏斗 ; 先将分液漏斗颈上的玻璃塞打开(或先使塞上的凹槽对准漏斗上的小孔),再将分液漏斗下面的活塞拧开;
( 3 ) SO 与钡离子反应生成不溶于强酸的硫酸钡沉淀,据此可检验硫酸根离子 , 所以检验滤液中 SO
的实验操作为:取少量滤液于小试管中 , 滴加少量盐酸酸化的 BaCl2 溶液 , 若有白色沉淀产生 , 说明含有 SO
,故答案为:取少量滤液于小试管中,滴加足量盐酸酸化无明显现象,再加入 BaCl 2 溶液,若有白色沉淀产生,说明含有 SO
;
( 4 )质量分数为 98 %、密度为 1.84g·cm -3 的浓硫酸的物质的量浓度为: =18.4mol/L ,则需要浓硫酸的体积为:
=13.6mL 。


 的检验:
的检验: ,
, 具有不溶于盐酸、硝酸的特性。
具有不溶于盐酸、硝酸的特性。 溶液或
溶液或 溶液,盐酸和稀硝酸。
溶液,盐酸和稀硝酸。  、
、 等判成SO42-,此时上述离子会分别产生
等判成SO42-,此时上述离子会分别产生 等白色沉淀.
等白色沉淀. 等判成SO42-,如向待测液中先滴加
等判成SO42-,如向待测液中先滴加 溶液,再加盐酸有白色沉淀生成便断定含SO42-。其错误之处是未注意溶液中不含SO42-而含Ag+或
溶液,再加盐酸有白色沉淀生成便断定含SO42-。其错误之处是未注意溶液中不含SO42-而含Ag+或 也会有同样现象,因为
也会有同样现象,因为

 判成
判成 ,如向待测液中滴加盐酸酸化的
,如向待测液中滴加盐酸酸化的 溶液,或滴加硝酸酸化的
溶液,或滴加硝酸酸化的 ,错在未注意
,错在未注意 在酸性条件下具有强氧化性,可将
在酸性条件下具有强氧化性,可将
 的检验常用气体法:
的检验常用气体法: (不能用硝酸等强氧化性酸),生成能使品红溶液褪色的无色有刺激性气味的气体。
(不能用硝酸等强氧化性酸),生成能使品红溶液褪色的无色有刺激性气味的气体。  的检验
的检验  ,所用酸必须是非强氧化性酸,可用稀盐酸或稀硫酸,生成能使湿润的醋酸铅试纸变黑的气体。
,所用酸必须是非强氧化性酸,可用稀盐酸或稀硫酸,生成能使湿润的醋酸铅试纸变黑的气体。  ,生成黑色沉淀;或
,生成黑色沉淀;或 ,生成乳白色或黄色沉淀(溶液中)。
,生成乳白色或黄色沉淀(溶液中)。 ”表示。
”表示。 





 。
。 。
。  等亚硫酸盐易溶于水、易电离。
等亚硫酸盐易溶于水、易电离。