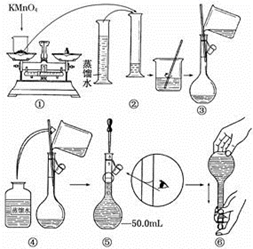
某化学实验室需要 480mL , 0.5mol/L 的稀硫酸,现欲用 18.4mol/L 的浓硫酸配制,配制步骤包括: ①计算所用浓硫酸的体积 ②转移 ③定容、摇匀 ④量取一定体积的浓硫酸 ⑤洗涤 ⑥稀释并冷却至室温 ⑦轻摇。完成下列问题:
(1) 正确的操作步骤为 ( 填入序号 ) ___ 。选用的主要仪器有:量筒、烧杯、玻璃棒、 __ 、 ____ 。
(2) 应量取浓硫酸的体积为 ___ ;量取浓硫酸所用的量筒的规格是 ___ ( 从下列中选用 A . 10 mL B . 25 mL C . 50 mL D . 100 mL) 。
(3) 下列关于容量瓶的使用方法中,正确的是 ____ 。
A .使用前要检验是否漏水 B .在容量瓶中直接溶解固体或稀释液体
C .溶液未经冷却即注入容量瓶中 D .向容量瓶中转移溶液要用玻璃棒引流
(4) 下列情况中,所配制的稀硫酸浓度偏大的是 ____ 。
A .所用的浓硫酸长时间放置在密封不好的容器中
B .容量瓶用蒸馏水洗涤后残留有少量的水
C .所用过的烧杯、玻璃棒未洗涤
D .定容时俯视刻度线
E .洗涤量取浓硫酸使用的量筒,并将洗涤液转移入容量瓶
F .用量筒量取浓硫酸时仰视刻度
答案
①④⑥②⑤⑦③ 500mL 容量瓶 胶头滴管 13.6 B AD DEF
【详解】
( 1 )配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解(冷却)、转移、洗涤、定容、摇匀、装瓶贴签等操作,所以正确的操作顺序为: ①④⑥②⑤⑦③;用到的仪器有:量筒、烧杯、玻璃棒、 500ml 容量瓶、胶头滴管,故还缺少的仪器为 500ml 容量瓶、胶头滴管;
( 2 )设需要 18.4mol/L 的浓硫酸体积为 V ,则依据溶液稀释规律,稀释前后的物质的量不变可得: 18.4mol/L×V=0.5mol/L×0.5L ,解得 V 0.0136mL=13.6mL ,故需量取 13.6mL 浓硫酸;依据 “ 大而近 ” 原则应选择 25mL 量筒,故选 B ;
( 3 ) A .容量瓶使用前要检验是否漏水, A 正确;
B .容量瓶不能用来稀释浓溶液或溶解固体,只能用来配制溶液, B 错误;
C .溶液未经冷却即注入容量瓶中,导致溶液体积偏小,配制浓度偏大, C 错误;
D .向容量瓶中转移溶液要用玻璃棒引流,防止液体溅出, D 正确;
故选 AD ;
( 4 ) A .所用的浓硫酸长时间放置在密封不好的容器中,浓硫酸会吸水,导致浓硫酸浓度降低,溶质的物质的量偏小,溶液浓度偏低, A 不符合题意;
B .容量瓶用蒸馏水洗涤后残留有少量的水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变, B 不符合题意;
C .所用过的烧杯、玻璃棒未洗涤,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低, C 不符合题意;
D .定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高, D 符合题意;
E .洗涤量取浓硫酸使用的量筒,并将洗涤液转移入容量瓶,导致硫酸的物质的量偏大,溶液浓度偏高, E 符合题意;
F .用量筒量取浓硫酸时仰视刻度,导致浓硫酸体积偏大,溶质的物质的量偏大,溶液浓度偏高, F 符合题意;
故选 DEF 。