高纯超细氧化铝是一种新型无机功能材料,以硫酸铵和硫酸铝为原料制备复盐硫酸铝铵 ![]() ,经硫酸铝铵热分解可制得高纯超细氧化铝,其流程如下:
,经硫酸铝铵热分解可制得高纯超细氧化铝,其流程如下:

回答下列问题:
(1) 操作 ①需加入稀 H 2 SO 4 ,其目的是 ___________ 。
(2) “纯化”的方法为 ___________ 。
(3) 实验室用如图装置利用热分解法制备高纯超细氧化铝粉并对其分解气成分进行探究:
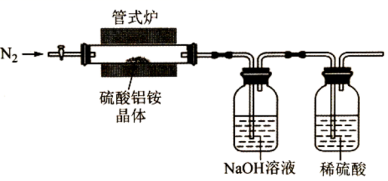
反应一段时间后,取三份 NaOH 吸收液于三支试管中分别进行如下实验,填写下表:
| 实验步骤 | 实验现象 | 实验结论 |
| ①加热,将湿润的红色石蕊试纸置于试管口 | 试纸变蓝 | 分解气中含有 ___________ |
| ②加入盐酸酸化,再滴加氯化钡溶液 | 产生白色沉淀 | 分解气中 ___________ |
| ③ ___________ | ___________ | 分解气中不含有 SO 2 |
写出硫酸铝铵晶体高温分解的化学方程式 ___________ 。
(4) 为了测定高纯超细氧化铝粉中 Al 2 O 3 的质量分数,可用 EDTA( 简写为 H 4 Y) 标准溶液滴定。取 mg 氧化铝粉溶于盐酸,加入过量的 V 1 mLc 1 mol·L -1 EDTA 标准溶液,充分反应后,再用 c 2 mol·L -1 的 Zn 2+ 标准溶液滴定过量的 EDTA 至终点,消耗 Zn 2+ 标准溶液体积为 V 2 mL 。反应的离子方程式: Al 3+ +Y 4- =AlY - 、 zn 2+ +Y 4- =ZnY 。 Al 2 O 3 的质量分数为 ___________ 。
抑制铵根离子和铝离子水解 重结晶 NH 3 SO 3 取部分吸收液,加入稀盐酸,将产生气体通入品红溶液中 品红溶液红色不褪去
【分析】
将原料中的硫酸铝铵溶解,制得硫酸铝铵溶液,经过蒸发浓缩冷却结晶后,过滤得到含有结晶水的硫酸铝铵粗品,将含有结晶水的硫酸铝铵粗品进行纯化,得到 ,经过热分解得到 Al 2 O 3 。
【详解】
(1) 由 ①前后物质可知为溶液到相应晶体的过程,没有与硫酸发生化学反应,且铵根离子和铝离子会水解,温度越高、水解程度越大,水解会生成氢离子,故加入硫酸的目的为抑制铵根离子和铝离子水解;
(2) 纯化前为粗品固体,纯化后为晶体,提纯固体粗产品物质常用重结晶,故答案为重结晶;
(3) ①红色石蕊试纸变蓝,说明气体呈碱性,故为 NH 3 ; ②硫酸钡为不溶于稀盐酸的白色沉淀,故分解气中有 SO 3 ; ③二氧化硫溶于氢氧化钠生成 Na 2 SO 3 ,故答案为取部分吸收液,加入稀盐酸,将产生气体通入品红溶液中,品红溶液红色不褪去,说明不含 SO 2 ;硫酸铝铵晶体高温分解的化学方程式为 ;
(4) 铝离子和锌离子物质的量之和与 EDTA 相等,即 n(Al 3+ )+n(Zn 2+ )=n(EDTA) ; n(Al 3+ )=( c 1 v 1 ×10 -3 -c 2 v 2 ×10 -3 )mol ,故 m(Al 3+ )=n(Al 3+ )·M=( c 1 v 1 ×10 -3 -c 2 v 2 ×10 -3 )mol×102g/mol=51×(c 1 v 1 ×10 -3 -c 2 v 2 ×10 -3 ) ,所以质量分数 = 。
定量实验介绍:


①实验开始时,首先要通入一段时间的氧气,目的是排除体系中的N2。
②D装置的作用是吸收未反应的O2,保证最终收集的气体是N2。
③读取N2体积时,应注意:量筒内液面与广口瓶中的液面相持平视线与凹液面最低处相切。
④实验中测得N2的体积为VmL(已折算为标准状况)。为确定此氨基酸的分子式,还需要的有关数据为生成二氧化碳气体的质量、生成水的质量、氨基酸的相对分子质量
(2)用氨气还原氧化铜的方法测定铜的近似相对原子质量实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为:2NH3+3CuO
 N2+3Cu+3H2O
N2+3Cu+3H2O(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。
装置图:

①连接顺序为:bcacd
②d中浓硫酸的作用是吸收未反应的氨、防止空气中水分进入;实验完毕时观察到a中的现象是固体由黑色转变为红色;
③Cu的相对原子质量的表达式

实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现按下图所示装置进行实验。

①实验开始时,首先要通入一段时间的氧气,目的是排除体系中的N2。
②D装置的作用是吸收未反应的O2,保证最终收集的气体是N2。
③读取N2体积时,应注意:量筒内液面与广口瓶中的液面相持平视线与凹液面最低处相切。
④实验中测得N2的体积为VmL(已折算为标准状况)。为确定此氨基酸的分子式,还需要的有关数据为生成二氧化碳气体的质量、生成水的质量、氨基酸的相对分子质量
用氨气还原氧化铜的方法测定铜的近似相对原子质量:
实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为:2NH3+3CuO
 N2+3Cu+3H2O
N2+3Cu+3H2O(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。
装置图:

①连接顺序为:bcacd
②d中浓硫酸的作用是吸收未反应的氨、防止空气中水分进入;实验完毕时观察到a中的现象是固体由黑色转变为红色;
③Cu的相对原子质量的表达式

2、掌握吸收法、滴定分析法、沉淀法等测定物质组成或含量的基本操作。
3、了解物质含量测定的现实意义。
课时要求:60
考试频率:常考
分值比重:4