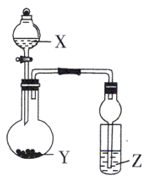
利用如图所示装置进行实验,将液体 X 逐滴加入到固体 Y 中。下列有关实验现象或结论正确的是
| 选项 | X | Y | Z | 实验现象或结论 | 装置 |
| A | 稀硫酸 | 亚硫酸钠 | 品红溶液 | | |
| B | 双氧水 | | 氢硫酸溶液 | 产生浑浊 | |
| C | 浓盐酸 | 石灰石 | 硅酸钠溶液 | 非金属性: | |
| D | 浓硝酸 | | 水 ( 含酚酞 ) | 试管中液体变红 |
A . A B . B C . C D . D
答案
B
【详解】
A .稀硫酸与亚硫酸氢钠溶液反应生成 SO 2 , SO 2 具有漂白性,能和品红溶液反应成一种不稳定的物质,漂白品红溶液,利用的不是 SO 2 的氧化性,故 A 错误;
B .双氧水是过氧化氢溶液的俗称,氢硫酸是硫化氢的水溶液,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为: 2H 2 O 2 2H 2 O+O 2 ↑,氧气能够将硫化氢氧化成 S 单质,从而使 B 中出现浑浊现象,故 B 正确;
C .石灰石为碳酸钙,碳酸钙与盐酸反应为: CaCO 3 +2HCl=CaCl 2 +H 2 O+CO 2 ↑,生成的 CO 2 中混有 HCl ,二者与硅酸钠反应都能生成硅酸沉淀,且 HCl 不是最高价氧化物,则不能证明非金属性: ,故 C 错误;
D . Cu 和浓硝酸反应生成 NO 2 , NO 2 和水反应生成 HNO 3 ,不能使试管中液体变红,故 D 错误;
故选 B 。


 2SO3
2SO3





 无色溶液
无色溶液 恢复原色。
恢复原色。


 ,如下数轴所示:
,如下数轴所示:
 则固体物质为Na2SO3,
则固体物质为Na2SO3, ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3. ,则同体物质为NaHSO3
,则同体物质为NaHSO3 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3, ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。