(1) 短周期中,金属性最强的元素是 ___________ ( 写元素符号,下同 ) ,非金属性最强的元素是 ___________ ,原子半径最小的元素是 ___________ 。
(2) 寻找所需元素:在 ___________ 区域找到制造半导体材料,如 ___________ ( 写元素符号 ) ;
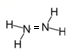
(3) 写出下列物质的电子式: NaOH ___________ ; N 2 ___________ ; Na 2 O 2 ___________ ; CO 2 ___________ ; NH 4 Cl ___________ ; HClO ___________ 。
(4) 现有下列几种微粒: 1 H 、 2 H 、 3 H 、 1 H + 、 234 U 、 235 U 、 238 U 、 40 K 、 40 Ca 、 Cl 2 、 14 N 、 14 C ,以上微粒分别属于 ___________ 种元素,互为同位素的原子分别为 ___________ 、 ___________ 。
答案
Na F H 金属和非金属分界线附近 Si 、 Ge ![]()
![]()
![]()
![]()
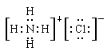
![]() 7 1 H 、 2 H 、 3 H 234 U 、 235 U 、 238 U
7 1 H 、 2 H 、 3 H 234 U 、 235 U 、 238 U
【详解】
(1) 元素周期表左下角的元素金属性最强,则短周期中,金属性最强的元素是 Na ;元素周期表中稀有气体原子最外层为稳定结构,不易得电子,非金属性弱,除稀有气体元素外右上角的元素非金属性最强,则短周期中,非金属性最强的元素是 F ;同主族从上向下原子半径增大,同周期从左往右原子半径减小,则短周期中原子半径最小的元素是 H ;
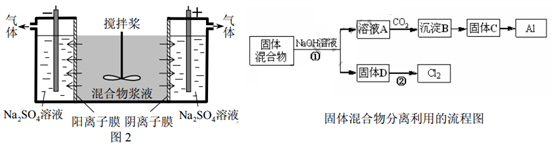
(2) 寻找所需元素:在金属与非金属分界线附近找到制造半导体材料,如 Si 、 Ge ;
(3)NaOH 是含共价键的离子化合物,其电子式为 ![]() ; N 2 分子中两个 N 形成三对共用电子,其电子式为
; N 2 分子中两个 N 形成三对共用电子,其电子式为 ![]() ; Na 2 O 2 是含共价键的离子化合物,其电子式为
; Na 2 O 2 是含共价键的离子化合物,其电子式为 ![]() ; CO 2 中 2 个 C 和 O 分别形成两对共用电子,其电子式为
; CO 2 中 2 个 C 和 O 分别形成两对共用电子,其电子式为 ![]() ; NH 4 Cl 是含共价键的离子化合物,其电子式为
; NH 4 Cl 是含共价键的离子化合物,其电子式为 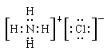 ; HClO 中 O 在中间,电子式为
; HClO 中 O 在中间,电子式为 ![]() ;
;
(4) 以上微粒分别属于 H 、 U 、 K 、 Ca 、 Cl 、 N 、 C 共 7 种元素;质子数相同、中子数不同的同种元素的不同种原子互为同位素,因此互为同位素的原子分别为 1 H 、 2 H 、 3 H , 234 U 、 235 U 、 238 U 。


 D
D