如表是元素周期表的一部分。
| 族 周期 | | | | | | | |
| | ① | | |||||
| | Li | | | C | ② | ③ | ④ |
| | ⑤ | ⑥ | ⑦ | ⑧ | | ⑨ | ⑩ |
(1) 表中元素的非金属性最强 ___ ( 填写元素符号,下同 ) ;原子半径最大的是元素 ___ ;其氧化物是两性氧化物的元素是 ___ 。
(2) 表中元素 ⑤和③、①和⑤均可以组成原子比例为 1 : 1 的物质,这两种物质内所含有的相同的化学键是 ___ 键 ( 填写 “ 离子键 ” 、 “ 极性共价键 ” 或 “ 非极性共价键 ”)
(3) 表中元素 ②③④氢化物的稳定性由大到小的顺序为: ___ ( 填写化学式,下同 ) 。
(4) 表中有一种元素的氧化物可作光导纤维材料,它在元素周期表中的位置是 ___ 。
(5) 用电子式表示表中 ③⑥两元素形成化合物的过程 ___ 。
答案
F Na Al 离子键 HF>H 2 O>NH 3 第三周期 Ⅳ A 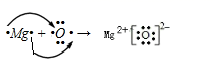
【分析】
根据元素周期表提供信息可知: ①为 H , ②为 N , ③为 O , ④为 F , ⑤为 Na , ⑥为 Mg , ⑦为 Al , ⑧为 Si , ⑨为 S , ⑩为 Cl ;据以上分析解答。
【详解】
(1) 同一周期从左到右,原子半径逐渐减小,非金属性增强,同一主族,从上到下,原子半径逐渐增大,非金属性减弱,因此表中元素的非金属性最强的是 F ;原子半径最大的是元素是 Na ;氧化铝既能与酸反应又能与碱反应,具有两性,所以氧化物是两性氧化物的元素是 Al ;
(2) 表中元素 ⑤和③、①和⑤均可以组成原子比例为 1 : 1 的物质,这两种物质分别为: Na 2 O 2 、 NaH ; Na 2 O 2 属于离子化合物,既含离子键又含非极性共价键, NaH 属于离子化合物,只含有离子键;所以这两种物质含有相同的化学键为离子键;
(3) 表中元素 ②③④氢化物的化学式为: NH 3 、 H 2 O 、 HF ;元素的非金属性越强,氢化物越稳定,非金属性: F>O>N ,所以氢化物的稳定性由大到小的顺序为: HF>H 2 O>NH 3 ;
(4) 二氧化硅具有良好的光学效应,可作光导纤维材料,硅元素为 14 号元素,在元素周期表中的位置是第三周期 ⅣA ;
(5) ③⑥两元素形成化合物为 MgO ,属于离子化合物,镁原子失电子转移给氧原子,用电子式表示 MgO 形成化合物的过程如下: 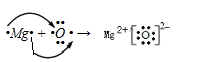 。
。
